現在の研究内容
当研究室では、「各種病態の解明」と「創薬」を目的としてプロジェクトを進めています。新たに見出された生体内の機能分子を標的とする医薬品を開発するための新しいアイデアを世界に発信したいと考えています。
○ T型カルシウムチャネルに関する研究
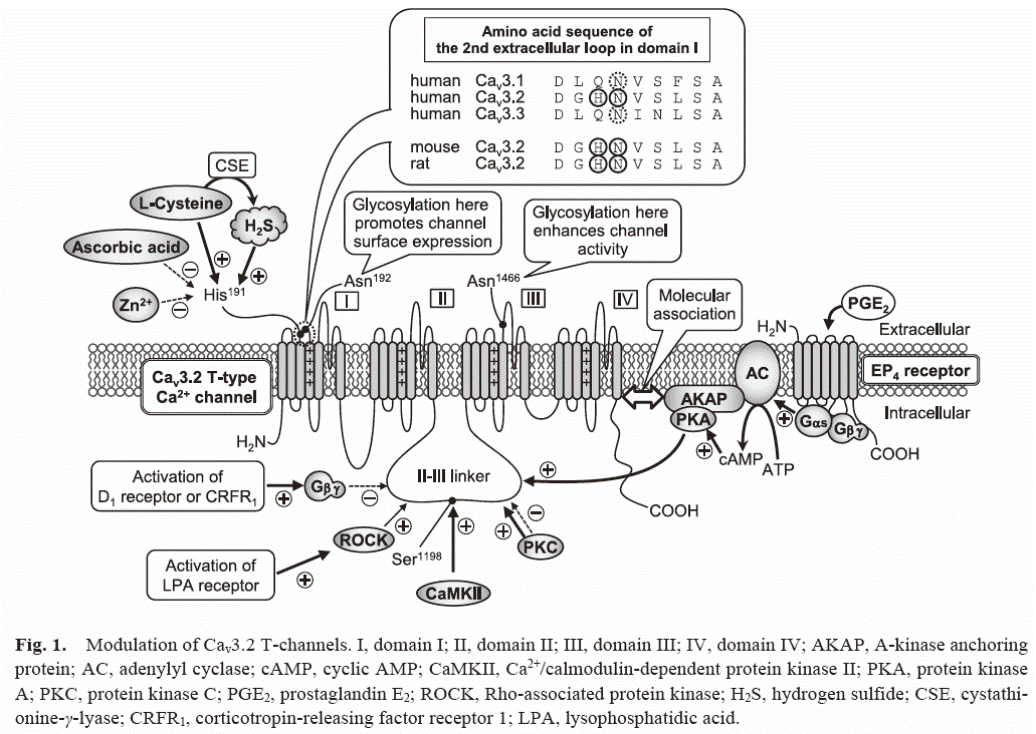
第3の気体メッセンジャーであることが明らかとなったH2Sが、Cav3.2 T型カルシウムチャネルの機能を高めることで痛みの情報伝達、神経軸索再生、炎症反応調節などにおいて多様な役割を演じていることを明らかにし、現在は、他大学の研究室や企業とも協力し、このCav3.2を標的とする医薬品の開発を進めています。
Free Review Article:
Sekiguchi
and Kawabata, J Pharmacol Sci 122, 244-250 (2013) https://www.jstage.jst.go.jp/article/jphs/122/4/122_13R05CP/_article
Schemes shown in articles:
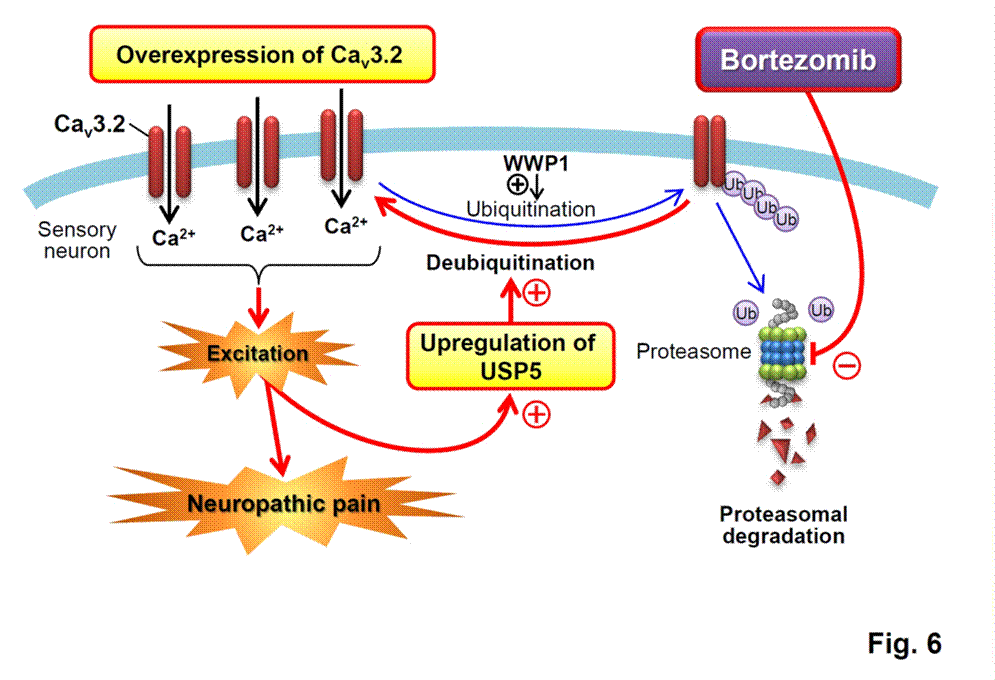
Tomita, S., Sekiguchi, F., Deguchi, T.,
Miyazaki, T., Ikeda, Y., Tsubota, M., Yoshida, S., Nguyen, H.D., Okada, T.,
Toyooka, N., Kawabata, A., Toxicology 413, 33-39 (2019) https://www.ncbi.nlm.nih.gov/pubmed/30552955
○PARに関する研究
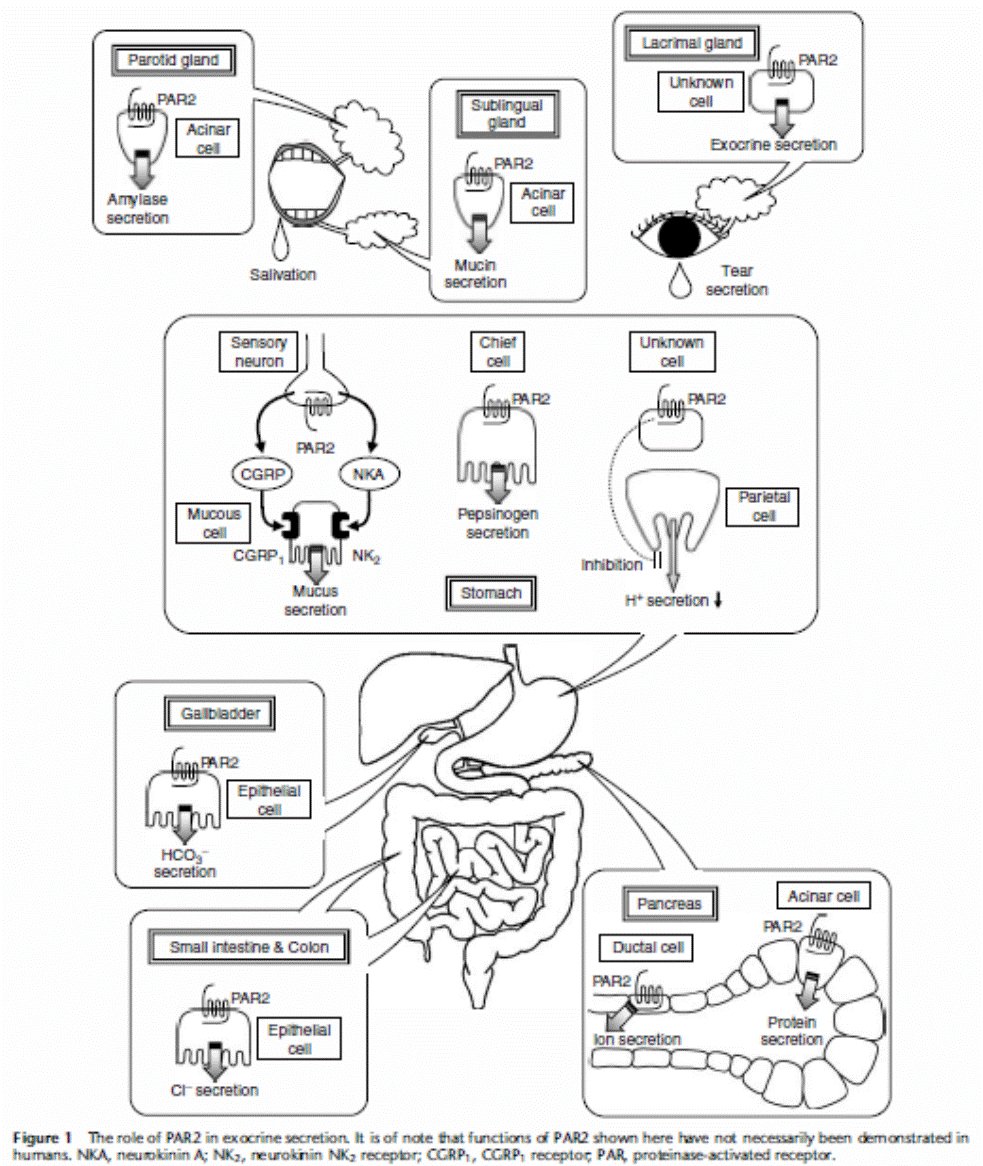
PARに関する研究は1997年から始まり、現在も続いています。この間、炎症、体性痛・内臓痛、胃粘膜機能制御、循環制御、唾液・涙液分泌、呼吸機能調節、膵機能制御、胃腸平滑筋運動調節など多様な生体内現象におけるPARの役割を世界に先駆けて発表し、この分野における研究をリードしてきました。最近は、PARの生理機能や病態への関与についての研究に加え、各種細胞においてPAR活性化により誘起される細胞シグナルの解明やPARに関する臨床研究にも取組んでいます。
Review Article:
Kawabata,
Matsunami, Sekiguchi, Br J Pharmacol Suppl 1, S230-S240 (2008) http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2268065/
○HMGB1に関する研究
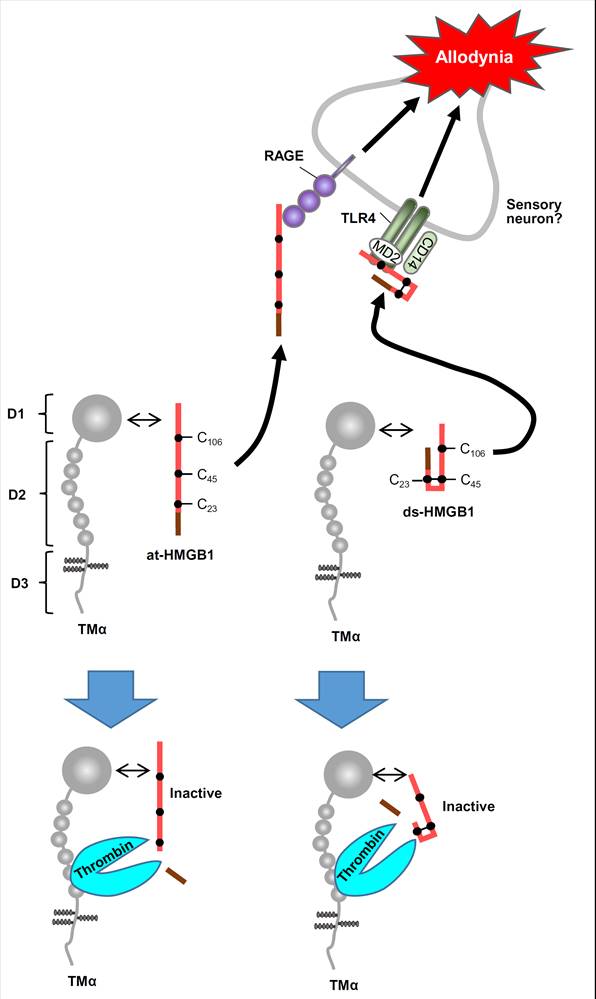
Damage-associated molecular patterns (DAMPs)の1つであるhigh mobility group box 1 (HMGB1)が、痛みの情報伝達に関与することを見出し、それを不活性化するヒト可溶性トロンボモジュリンが痛みを抑制することを明らかにしました。
Schemes shown in articles:
u Tsujita, Tsubota, Hayashi, Saeki,
Sekiguchi, Kawabata, J Neuroimmune Pharmacol, in press (2018) https://www.ncbi.nlm.nih.gov/pubmed/29196860
☆トロンボモジュリンアルファによるHMGB1誘起アロディニアの抑制は、トロンビン依存性である。
u Hayashi, Tsujita, Tsubota, Saeki,
Sekiguchi, Honda, Kawabata, Biochem Biophys Res Commun 495, 634-638 (2018)
(2018) https://www.ncbi.nlm.nih.gov/pubmed/29146186
☆トロンボモジュリンアルファによるHMGB1誘起アロディニアの抑制にはD1およびD2両ドメインが結合した状態にあることが必要である。
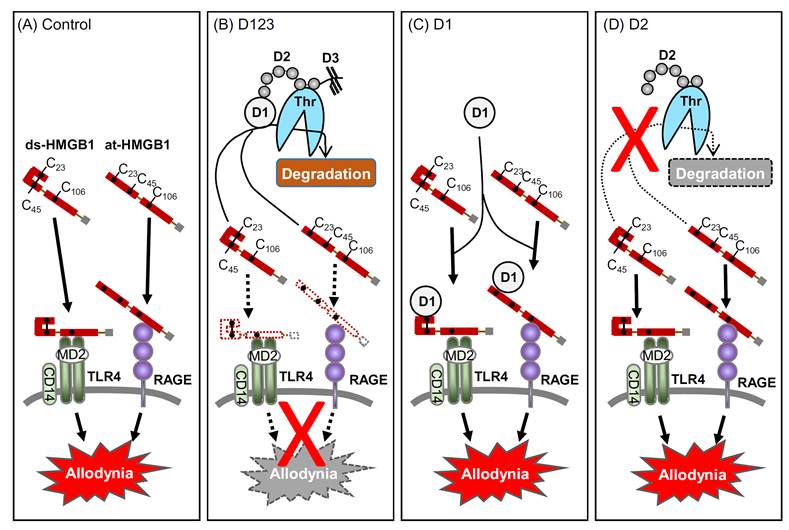
u
Sekiguchi,
Domoto, Nakashima, Yamasoba, Yamanishi, Tsubota, Wake, Nishibori, Kawabata,
Neuropharmacology 141, 201-213 (2018) https://www.ncbi.nlm.nih.gov/pubmed/30179591
☆パクリタキセル誘起末梢神経障害にはマクロファージ由来HMGB1が関与する。
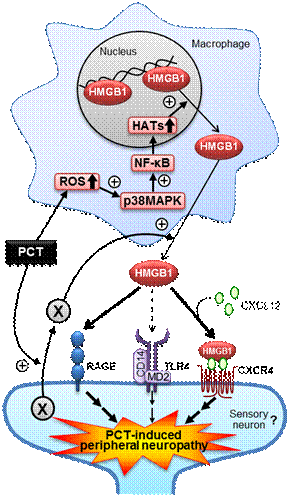
○痛みの情報伝達メカニズムに関する研究
上記PAR, H2S, T型カルシウムチャネルに加えて、プロスタグランジンE2, 核内タンパクHMGB1などの分子の疼痛情報伝達における役割を明らかにするための検討を行っています。天然物由来の生理活性物質を含む新規化合物の中から、難治性疼痛に対する治療薬を開発するのが最終目標です。
Free Review Article:
u Kawabata, Biol Pharm Bull 34,
1170-1173 (2011) https://www.jstage.jst.go.jp/article/bpb/34/8/34_8_1170/_article
☆末梢組織中PGE2による痛みの促進に関与する分子メカニズム
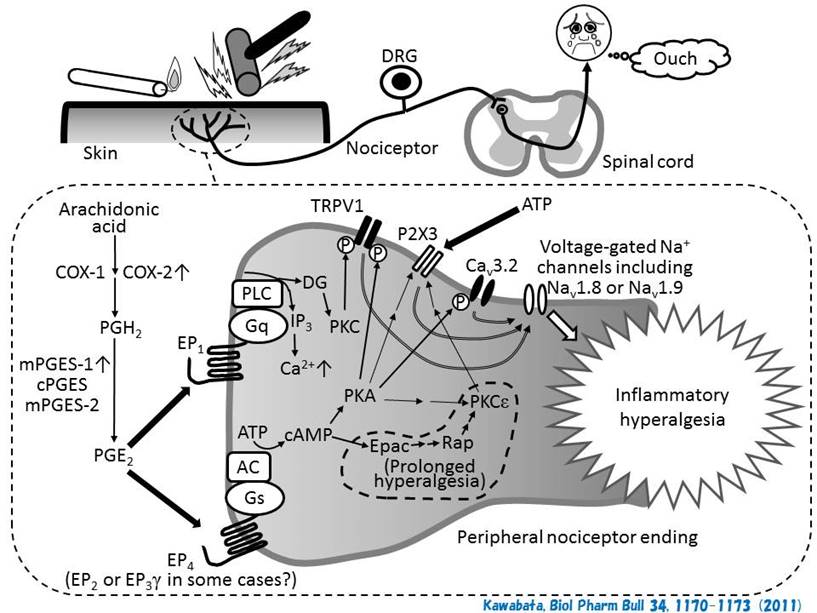
Review Article:
u 坪田真帆、川畑篤史 膵炎の疼痛における侵害受容体の関与と治療への展望.胆と膵 37 (12), 1535-1539(2016)
☆膵臓痛の分子メカニズム
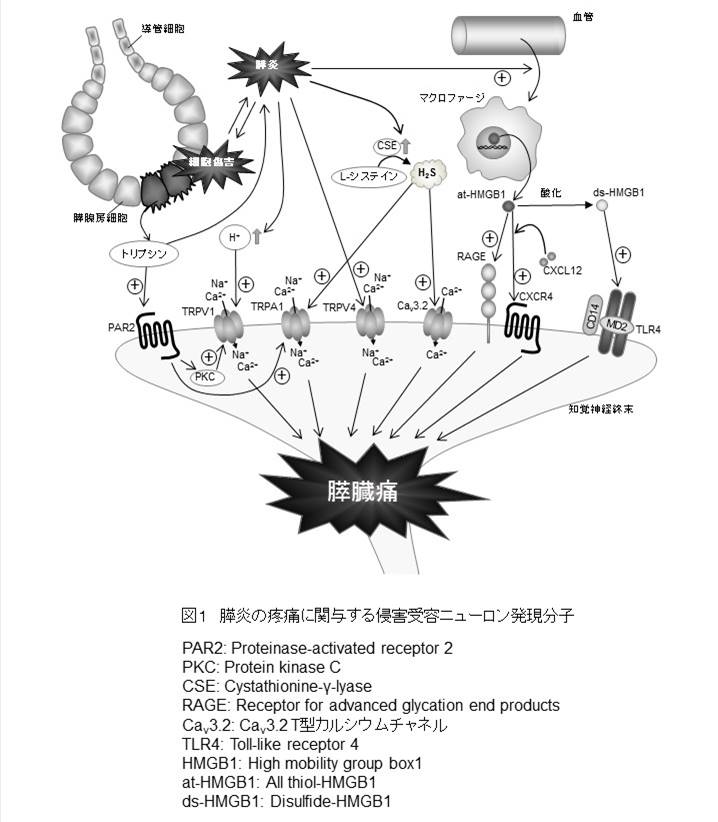
○麻薬、覚醒剤、大麻成分に関する研究
がん性疼痛の治療に重要なモルヒネを含む麻薬性鎮痛薬に関する研究のほか、大麻成分カンナビノイドの受容体CB1およびCB1を刺激する薬物の治療応用、さらに、覚醒剤の毒性や逆耐性現象の分子メカニズムに関する研究も進めています。