細胞内で物質運搬に関わる重要なタンパク間の連携を発見
ゲノム科学と遺伝薬理学の手法を用いて解明
〜がん化の解明にも手がかり〜
近畿大学薬学部 分子医療・ゲノム創薬学研究室
杉浦麗子教授グループ
概要
細胞内で物質や脂質を運ぶ際には、小胞体からゴルジへ、そしてゴルジから細胞膜へと輸送物質が運ばれます。物質の運搬は様々なタンパク質が関わりながら、リレーのような形で、物質の受け渡しを行います。物質の運搬がうまくいかないと、細胞の形が異常になり、細胞のがん化にもつながります。
低分子量Gタンパク質Rhoは、細胞内で様々な標的タンパク質との連携により、物質運搬の鍵を握る重要なタンパク質ですが、その仕組みの多くは謎に包まれていました。また、人においてRhoの働きが異常になることで、細胞骨格・形態の異常やがん化が引き起こされることから、Rhoの働きに狙いを絞った薬物の開発は、抗がん薬の創製という意味からも注目されています。
杉浦研究チームは、現在までにクラスリンアダプター複合体が細胞内の物質運搬に重要であることを突き止めていましたが(米科学誌Molecular Biology of the Cell)、今回新たにRhoの一種であるRho3とクラスリンアダプター複合体の連携を発見しました。
杉浦教授のグループは、ゲノム科学と遺伝薬理学の手法を用いて「クラスリンアダプター複合体」とRho3が結合し、協力しながら、ゴルジ体における物質の運搬を調節するという仕組みを見つけました。
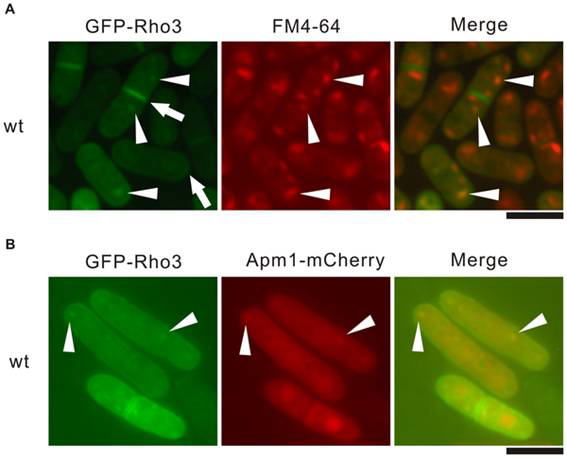
研究チームは、クラスリンアダプター複合体の機能が低下した特殊な細胞をゲノム薬理学の手法で作製し、この細胞の働きを補うことのできる遺伝子としてRho3を発見しました。さらに、杉浦教授研究チームの喜多助教らは、電子顕微鏡を用いて高解像度で細胞の構造を観察し、Rho3の働きを失った細胞では、異常に肥厚したゴルジ体や、運搬されない物質がゴルジ体の近くに蓄積していることも明らかにしました(図1参照)。これは、Rho3タンパク質がゴルジ体の物質の運搬に重要な役割をしていることを強く示唆しています。しかも、クラスリンアダプター複合体とRho3は、どちらもゴルジ体に局在し、結合することも明らかにしました(図2)。
さらに研究チームは、高度なゲノム科学のテクニックを用いて、Rho3とクラスリンアダプター複合体の働きを同時に失わせることにより、細胞が死滅することも明らかにしました。
本研究で用いたRho3は、分裂酵母というヒトと同じ真核生物に属する微生物のタンパク質ですが、人間にもRho3と非常に良く似たRhoタンパク質が存在し、物質の運搬や細胞の形態形成、がんの発症や転移に関わっています。
今回の研究成果は、細胞のがん化や転移の仕組みを解明し、Rhoを標的とした新しい抗がん薬創製の手がかりとなる可能性があります。
本研究成果はその重要性と高いインパクトから、平成23年2月3日にアメリカ科学誌(PLoS ONE)の電子版に掲載されました。
図1 電子顕微鏡を用いたrho3遺伝子ノックアウト細胞内構造の解析
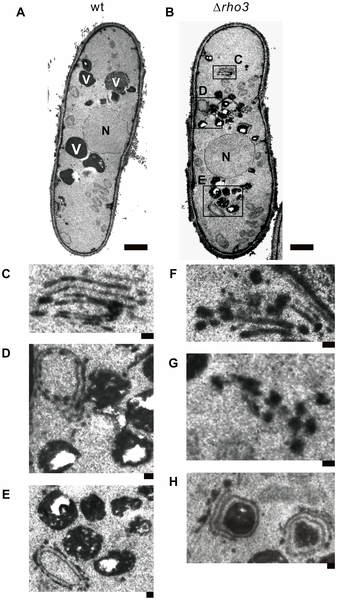
図2 GFP-Rho3とApm1-mCherryのゴルジ体における局在
低分子量Gタンパク質Rhoは、細胞内で様々な標的タンパク質との連携により、物質運搬の鍵を握る重要なタンパク質ですが、その仕組みの多くは謎に包まれていました。また、人においてRhoの働きが異常になることで、細胞骨格・形態の異常やがん化が引き起こされることから、Rhoの働きに狙いを絞った薬物の開発は、抗がん薬の創製という意味からも注目されています。
杉浦研究チームは、現在までにクラスリンアダプター複合体が細胞内の物質運搬に重要であることを突き止めていましたが(米科学誌Molecular Biology of the Cell)、今回新たにRhoの一種であるRho3とクラスリンアダプター複合体の連携を発見しました。
杉浦教授のグループは、ゲノム科学と遺伝薬理学の手法を用いて「クラスリンアダプター複合体」とRho3が結合し、協力しながら、ゴルジ体における物質の運搬を調節するという仕組みを見つけました。
研究チームは、クラスリンアダプター複合体の機能が低下した特殊な細胞をゲノム薬理学の手法で作製し、この細胞の働きを補うことのできる遺伝子としてRho3を発見しました。さらに、杉浦教授研究チームの喜多助教らは、電子顕微鏡を用いて高解像度で細胞の構造を観察し、Rho3の働きを失った細胞では、異常に肥厚したゴルジ体や、運搬されない物質がゴルジ体の近くに蓄積していることも明らかにしました(図1参照)。これは、Rho3タンパク質がゴルジ体の物質の運搬に重要な役割をしていることを強く示唆しています。しかも、クラスリンアダプター複合体とRho3は、どちらもゴルジ体に局在し、結合することも明らかにしました(図2)。
さらに研究チームは、高度なゲノム科学のテクニックを用いて、Rho3とクラスリンアダプター複合体の働きを同時に失わせることにより、細胞が死滅することも明らかにしました。
本研究で用いたRho3は、分裂酵母というヒトと同じ真核生物に属する微生物のタンパク質ですが、人間にもRho3と非常に良く似たRhoタンパク質が存在し、物質の運搬や細胞の形態形成、がんの発症や転移に関わっています。
今回の研究成果は、細胞のがん化や転移の仕組みを解明し、Rhoを標的とした新しい抗がん薬創製の手がかりとなる可能性があります。
本研究成果はその重要性と高いインパクトから、平成23年2月3日にアメリカ科学誌(PLoS ONE)の電子版に掲載されました。
図1 電子顕微鏡を用いたrho3遺伝子ノックアウト細胞内構造の解析

図2 GFP-Rho3とApm1-mCherryのゴルジ体における局在

分子医療・ゲノム創薬学研究室
〒577-8502
大阪府東大阪市小若江3-4-1
近畿大学薬学部
分子医療・ゲノム創薬学研究室
TEL 06-6721-2332(内線3850)
FAX 06-6730-1394